
Après avoir montré son utilité en 2020 dans le diagnostic et l’orientation éthiologique des PID, le nez électrique, ou eNose, est aujourd’hui envisagé comme outil pratique pour prédire la réponse au traitement.
En 2020, quand l’ERS était encore virtuel, l’équipe de l’Institut Erasmus de Rotterdam a présenté des données marquantes sur une technologie non invasive mesurant des composés organiques volatiles dans l’air expiré de patients : le nez éléctrique ou eNose (SpiroNoseâ). Une fois la correction appliquée pour s’affranchir de l’air ambiant, la signature recueillie apportait une sensibilité et une spécificité permettant les diagnostics positifs de pneumopathie interstitielle diffuse (PID) et une orientation étiologique (distinction sarcoïdoses des FPI, IPAF, PHS, PINS et PID de connectivite).
En 2022, et lors d’une session particulièrement riche sur les sujets chauds du moment dans les PID, la thématique a été déroulée par le Dr Van der Sar en s’intéressant cette fois ci à l’eNose comme marqueur pronostique de traitement. Dans un domaine où il n’y a actuellement aucun biomarqueur suffisamment performant pour prédire la réponse à des thérapeutiques coûteuses ou risquées, l’apport de l’eNose pourrait être un outil pratique de premier plan pour le clinicien.
Ainsi, ont été inclus des patients atteints de PID avant l’initiation d’un traitement anti-fibrosant (n=24 patients, 71% nintedanib, 29% pirfenidone) ou immunosuppresseur (n=29 patients, 46% prednisone, 28% mycophenolate mofetil, 21% méthotrexate). Une mesure de leur air exhalé via le dispositif eNose était pratiquée. Ils bénéficiaient ensuite d’un suivi clinique et spirométrique sous traitement, la réponse à 3 mois étant définie par une perte de CVF inférieure ou égale à 2,5% (anti-fibrosants) ou un gain de CVF supérieur ou égal à 5% (immunosuppresseurs).
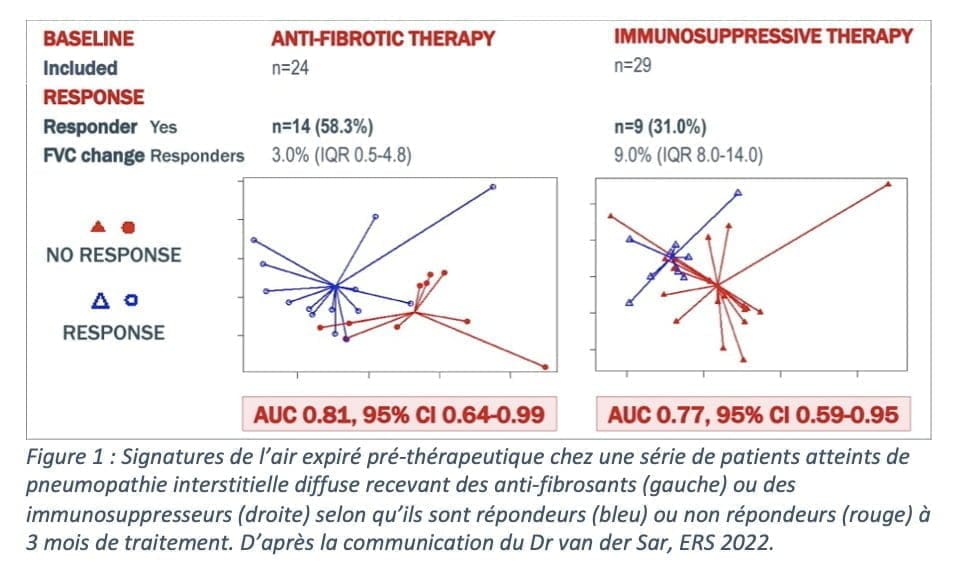
L’analyse comparative des patients, répondeurs versus non répondeurs, a permis d’identifier 2 profils aériques différents (cf. Figure 1). Les spécificité et sensibilité de l’eNose ont été évaluées par une analyse ROC. Ainsi, avec une aire sous la courbe de 0,81 (IC95% [0,64- 0,99]) pour les anti-fibrosants et de 0,77 (IC95% [0,59-0,95]) pour les immunosuppresseurs, l’analyse de l’air expiré par le dispositif eNose pourrait prédire la réponse au traitement avant même son initiation chez les patients atteints de PID.
Evidemment, des études de plus large envergure avec des populations plus homogènes sont nécessaires pour confirmer cette preuve de concept. Nul doute que nous en entendrons de nouveau parler dans l’avenir !
Clairelyne Dupin, Service de pneumologie A, Hôpital Bichat, Paris
D’après la presentation orale OA1391 « Predicting treatment response in patients with interstitial lung disease using electronic nose technology » par le Dr Iris G. Van der Sar – Session 173 “What is hot in interstitial lung diseases”, du dimanche 4 septembre 2022.



